23 januari 2019, door NCI Staff
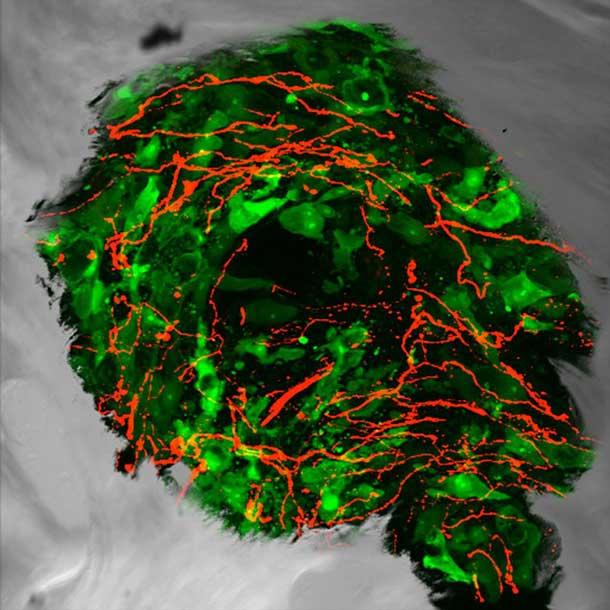
Zintuiglijke zenuwvezels (rood) ontspruiten in prostaattumorcellen (groen) die zijn uitgezaaid naar het bot.
Pijn is een veel voorkomend en gevreesd symptoom bij mensen die worden behandeld voor kanker en bij mensen die al lang leven. Kankerpijn kan worden veroorzaakt door de ziekte zelf, de behandelingen of een combinatie van beide. De pijn kan kortdurend of chronisch zijn, en bij sommige mensen kan de pijn nog lang na het einde van de behandeling aanhouden.
En steeds meer mensen leven met kankergerelateerde pijn. Dankzij verbeterde behandelingen leven mensen met gevorderde kanker langer en blijft het aantal overlevenden van kanker op de lange termijn toenemen. Omdat kanker bovendien vaker voorkomt bij oudere mensen, neemt de wereldwijde prevalentie van kanker toe naarmate mensen over de hele wereld langer leven.
De toegenomen prevalentie van kankerpijn en de gevolgen van de opioïdenepidemie voor de behandeling van kankerpijn – en voor de behandeling van chronische pijn in het algemeen – hebben een hernieuwde belangstelling gewekt voor de ontwikkeling van nieuwe, niet verslavende pijnmedicijnen en voor niet-medicamenteuze benaderingen voor de behandeling van chronische pijn.
Het begrijpen van kankerpijn is een uitdagend probleem, en het aantal onderzoekers dat op dit gebied werkzaam is, is klein, aldus Ann O’Mara, Ph.D., R.N., M.P.H., die onlangs met pensioen ging als hoofd van palliatief onderzoek in NCI’s Division of Cancer Prevention. Desondanks zijn wetenschappers die kankerpijn bestuderen voorzichtig optimistisch dat er betere behandelingen in het verschiet liggen.
Dankzij de ontwikkeling van diermodellen van sommige vormen van kankerpijn, beginnen onderzoekers de onderliggende biologie ervan beter te begrijpen. Met name identificeren wetenschappers moleculen die pijnsignalen opwekken en krijgen zij inzicht in de manier waarop het zenuwstelsel deze signalen van de pijnplek naar de hersenen stuurt, waar de pijn wordt waargenomen.
Dit onderzoek heeft geleid tot talrijke lopende klinische proeven, waaronder enkele grote studies die meestal nodig zijn om goedkeuring van de Food and Drug Administration te krijgen, van experimentele therapieën om pijn te voorkomen.
Inzichten over door kanker veroorzaakte botpijn die leiden tot nieuwe behandelingen
Eén van de meest voorkomende vormen van kankerpijn is botpijn. Door kanker veroorzaakte botpijn ontstaat wanneer uitgezaaide tumoren van kankers die in andere delen van het lichaam zijn begonnen, in het beenmerg groeien, het sponsachtige weefsel in het centrum van de meeste botten. In feite kan botpijn het eerste symptoom zijn van verschillende vormen van kanker, waaronder prostaat- en longkanker, aldus Patrick Mantyh, Ph.D., J.D., van de Universiteit van Arizona in Tucson.
Door kanker veroorzaakte botpijn komt ook voor bij mensen met primaire botkankers (tumoren die in het botweefsel beginnen), zoals osteosarcoom, die veel minder vaak voorkomen dan kankers die naar de botten uitzaaien.
In 1999 ontwikkelde het lab van Dr. Mantyh het eerste diermodel dat lijkt te weerspiegelen wat er bij mensen gebeurt met pijn als gevolg van kanker die naar de botten is uitgezaaid, of uitgezaaid. Met behulp van dat muismodel ontdekte het team van Dr. Mantyh dat tumoren in het bot de uitlopers van pijnoverbrengende zenuwvezels in de buurt van de tumor stimuleren.
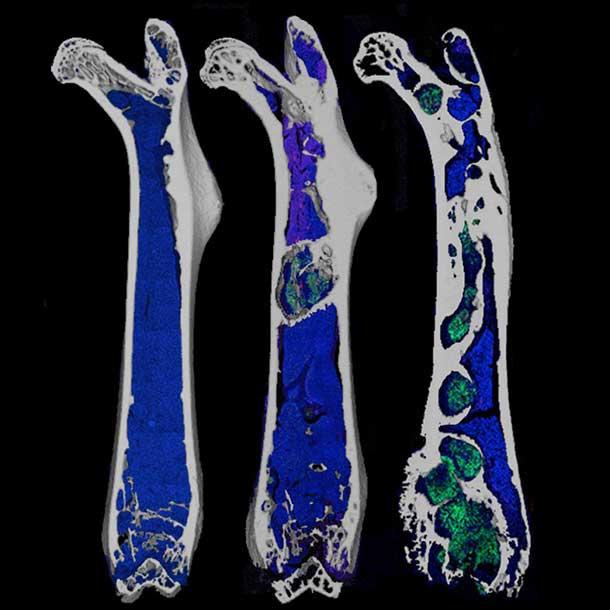
CT-beelden van een dijbeen in een vroeg (links), midden (midden) en laat (rechts) stadium van groei van prostaattumorcellen (groen) in het bot.
Als tumorcellen zich eenmaal in het beenmerg hebben gevestigd, kapen ze volgens dr. Mantyh de moleculen die de cellen reguleren die betrokken zijn bij het afbreken van bot, de zogenaamde osteoclasten. Het resultaat is dat “de osteoclasten groter worden en dan verteren ze gretig het bot,” legde hij uit.
Om het bot te verteren, creëren de osteoclasten een zure omgeving die “bijna lijkt op het gieten van accuzuur op het bot,” vervolgde Dr. Mantyh. De oorzaken van pijn door botkanker zijn tweeledig, zei hij. Ten eerste, sensorische neuronen, of zenuwvezels, in het bot “detecteren de zure omgeving en signaleren dit als pijn.” Ten tweede resulteert overmatige activiteit van osteoclasten in microfracturen of volledige botbreuken die extreme pijn kunnen veroorzaken.
Studies met behulp van het muismodel van het lab leidden tot proeven op mensen met denosumab (Prolia), het eerste geneesmiddel dat is goedgekeurd voor de behandeling van botpijn veroorzaakt door uitgezaaide kanker, en met bisfosfonaten zoals alendronaat (Fosamax), een andere eerstelijns therapie voor door kanker veroorzaakte botpijn. Zowel denosumab als bisfosfonaten, die oorspronkelijk werden ontwikkeld voor de behandeling van osteoporose, helpen de integriteit van de botten te behouden door de activiteit van de osteoclasten te remmen.
Een mogelijke nieuwe behandeling voor botpijn als gevolg van uitgezaaide kanker is een antilichaam genaamd tanezumab, dat de activiteit blokkeert van een pijnsignaalmolecuul dat zenuwgroeifactor (NGF) wordt genoemd. Dr. Mantyh’s team toonde bij muizen aan dat tanezumab de zenuwuitlopers in het bot blokkeert en de ontwikkeling van kankerpijn in een laat stadium vermindert.
Tanezumab wordt nu getest in fase 3 van klinische proeven voor door kanker veroorzaakte botpijn. Een verwante benadering probeert de werking van NGF te blokkeren door zijn receptor, bekend als TrkA (tropomyosin receptor kinase A), op sensorische zenuwvezels te blokkeren, zei Dr. Mantyh.
Er is ook grote belangstelling voor het gebruik van cannabinoïden – chemische stoffen uit marihuana – bij de behandeling van door kanker veroorzaakte botpijn en sommige andere vormen van kankerpijn, aldus Dr. O’Mara, hoewel het onderzoek op dit gebied tot nu toe beperkt is gebleven tot studies in diermodellen.
Er is bijvoorbeeld werk verricht door Todd Vanderah, Ph.D., van de Universiteit van Arizona, heeft aangetoond dat cannabinoïden ernstige botpijn kunnen verminderen en ook de groei van kanker kunnen onderdrukken en botverlies kunnen verminderen in een muismodel van borstkanker die is uitgezaaid naar het bot.
Kijken naar de oorzaken van pijn bij mondkanker
De meest voorkomende kankersoorten, zoals borst-, long-, prostaat- en darmkanker, veroorzaken zelden pijn op de plaats waar ze zijn ontstaan. Pijn in het hoofd en de nek als gevolg van mondkanker is echter opmerkelijk door zijn intensiteit en prevalentie, met ongeveer 70%-75% van de patiënten met mondkanker die pijn ervaren, zei Brian Schmidt, D.D.S., M.D., Ph.D., van New York University’s College of Dentistry.
Dr. Schmidt merkte op dat pijn bij mondkanker hardnekkig is omdat de tong en de bodem van de mond (de gebieden die het meest worden aangetast door mondkanker) worden verstoord wanneer een patiënt praat, kauwt of slikt. Pijn ontstaat wanneer stoffen die door een tumor worden geproduceerd en uitgescheiden nabijgelegen pijngevoelige neuronen activeren, die vervolgens pijnsignalen doorgeven aan het centrale zenuwstelsel – en de stimulatie van gewoon praten of slikken verergert dit effect.
Om de pijn bij mondkanker te bestuderen, verzamelt Dr. Schmidt tijdens operaties tumor geproduceerde, pijnveroorzakende stoffen met een techniek die microdialyse wordt genoemd. “Het kankerweefsel degenereert snel na de operatie. Door de kankermicro-omgeving te bemonsteren terwijl de tumor nog aanwezig is, krijgen we een beter inzicht in hoe de tumor pijn veroorzaakt”, aldus Dr. Schmidt.
In andere gevallen verwijdert Dr. Schmidt kleine stukjes tumor en normaal weefsel uit een aangrenzend deel van de mond. Aan de hand van deze monsters probeert zijn laboratorium de pijnveroorzakende stoffen te identificeren die wel in het kankerweefsel zitten maar niet in het normale weefsel.
Onze hoofdverdachten voor het veroorzaken van pijn bij mondkanker zijn proteasen-enzymen die eiwitten afbreken en kankers kunnen helpen zich te verspreiden door omliggend weefsel te vernietigen. Proteasen kunnen zich ook vastklampen aan een receptormolecuul op neuronen, protease-activated receptor 2 (PAR2) genaamd, en dit activeren. Wanneer proteasen PAR2 op neuronen activeren, kan PAR2 ervoor zorgen dat andere pijnreceptoren op neuronen gevoeliger worden, aldus Dr. Schmidt. Als gevolg hiervan, vervolgde hij, “kan een stimulus die normaal niet pijnlijk is, zoals een aardappelchip die tegen de tong slaat, buitengewoon pijnlijk worden.”
Dr. Schmidt en een medewerker, Nigel Bunnett, Ph.D., van Columbia University, bestuderen een nieuwe klasse medicijnen die PAR2 blokkeren om pijn bij mondkanker te behandelen. Daarnaast onderzoekt het team van Dr. Schmidt verschillende andere stoffen die kunnen bijdragen aan pijn bij mondkanker. Dit zijn onder andere NGF, een boosdoener bij kankergerelateerde botpijn, en endothelin-1, een pijnveroorzakende molecule die bekend staat om zijn aanwezigheid in slangengif.
Pijn als bijwerking van de behandeling

Pijn kan ook ontstaan als gevolg van chemotherapie-geïnduceerde perifere neuropathie (CIPN), een ernstige bijwerking van veel chemotherapie medicijnen. Perifere neuropathie ontstaat door beschadiging van zenuwen in de extremiteiten, zoals vingers en tenen, en veroorzaakt pijn, gevoelloosheid en tintelingen. (Kankerbehandelingen zoals chirurgie en bestraling, evenals de ziekte zelf, kunnen ook perifere neuropathie veroorzaken bij patiënten en overlevenden.)
CIPN is de meest voorkomende reden dat patiënten hun dosis chemotherapie moeten verminderen. Sommigen stoppen zelfs helemaal met de kankerbehandeling omdat de effecten van CIPN zo slopend en verontrustend zijn. En het is niet alleen het pijnlijke aspect van neuropathie dat problematisch is.
“De niet-pijnlijke componenten hebben ook grote invloed op het functioneren en het welzijn van de patiënt,” zegt Patrick Dougherty, Ph.D., van de afdeling pijngeneeskunde van het MD Anderson Cancer Center van de Universiteit van Texas.
Een recente studie onder leiding van Igor Spigelman, Ph.D., van de UCLA School of Dentistry, toonde aan dat een synthetische cannabinoïde de symptomen van CIPN onderdrukte bij zowel mannelijke als vrouwelijke ratten. Deze cannabinoïde is een van een reeks synthetische cannabinoïden die Dr. Spigelman en Herbert Seltzman, Ph.D., van het Research Triangle Institute in North Carolina, hebben ontwikkeld die geen invloed lijken te hebben op het centrale zenuwstelsel en die dus de cognitieve effecten vermijden die door andere cannabinoïden worden veroorzaakt, zoals euforie, verslaving en verminderde functie.
Er is slechts van één medicijn, duloxetine (Cymbalta), aangetoond dat het de pijn als gevolg van CIPN vermindert bij mensen in een fase 3 klinische studie, en dat effect is zeer bescheiden, zei Dr. Dougherty.
Wetenschappers begrijpen de mechanismen die ten grondslag liggen aan CIPN nog niet volledig, maar een combinatie van dierlijke en menselijke studies levert nieuwe inzichten op, voegde Dr. Dougherty eraan toe. Het algemene idee, legde hij uit, is dat de chemotherapie medicijnen die CIPN veroorzaken dit doen door neuronen te belasten, wat leidt tot zenuwontsteking en schade.
Onderzoekers onderzoeken middelen die de bron van het probleem kunnen aanpakken en CIPN kunnen omkeren of, idealiter, voorkomen in plaats van alleen de symptomen te verlichten. Sommige van deze middelen hebben ook bekende antitumor effecten, waardoor ze bijzonder aantrekkelijk zijn, omdat een belangrijk punt van zorg bij de ontwikkeling van geneesmiddelen ter voorkoming van CIPN is dat ze de behandeling van de kanker zouden kunnen verstoren.
“Sommige nieuwe soorten middelen komen naar klinische proeven, en op dit moment zijn de gegevens zeer veelbelovend,” zei Dr. Dougherty.
Drugs die de werking van histon deacetylase (HDAC) blokkeren, die al worden getest in klinische proeven voor hun potentieel om de effecten van chemotherapie te versterken, zijn slechts een van de vele mogelijke gerichte therapieën die worden onderzocht voor CIPN. Studies in diermodellen hebben aangetoond dat bepaalde HDAC-remmers CIPN kunnen voorkomen en omkeren.
Maar als het gaat om nieuwe geneesmiddelen voor de behandeling of preventie van CIPN, zei Dr. Dougherty, “zijn we nog steeds erg in een ontdekkingsmodus.”
Een rol voor niet-medicamenteuze benaderingen
Onderzoekers onderzoeken ook niet-medicamenteuze benaderingen voor het verlichten van CIPN en andere chronische kankergerelateerde pijn, legde Diane St. Germain, R.N. uit, M.S., die een subsidieportefeuille beheert die gericht is op palliatief onderzoek in de Division of Cancer Prevention van het NCI.
Er is bijvoorbeeld grote belangstelling voor het gebruik van acupunctuur, evenals gedragsbenaderingen zoals yoga, Tai Chi en mindfulness-meditatie, voor pijnverlichting, aldus Linda Porter, Ph.D., directeur van de Office of Pain Policy bij het National Institute of Neurological Disorders and Stroke, en veel van deze benaderingen worden getest in klinische proeven.
NIH Initiative to Spur Research on Non-Addictive Pain Treatments
Een initiatief waarvan wordt verwacht dat het het onderzoek naar nieuwe, veiligere behandelingsmogelijkheden voor pijnbestrijding in het algemeen zal versnellen, is het NIH Helping to End Addiction Long-term (HEAL) Initiative. Het verbeteren van de pijnbestrijding is een van de twee belangrijkste onderdelen van HEAL, dat het NIH heeft gelanceerd om wetenschappelijke oplossingen te bieden voor de opioïdencrisis. Dit onderdeel van HEAL zal onderzoek financieren om de volgende doelen te bereiken:
- Ontdek de biologische onderliggende factoren van chronische pijn
- Versnel de ontdekking en preklinische ontwikkeling van niet-verslavende pijnbehandelingen
- Versterk nieuwe niet-verslavende
- Het bevorderen van nieuwe niet-verslavende pijnbehandelingen in de klinische pijplijn
- Het vaststellen van de beste strategieën voor pijnbeheersing bij acute en chronische pijnaandoeningen
Gedragsinterventies bij kankerpijn worden over het algemeen gebruikt als aanvulling op medicatie, zegt Tamara Somers, Ph.D., een klinisch psycholoog en gedragswetenschapper aan de Duke University School of Medicine.
Dr. Somers bestudeert gedragsmatige pijnbeheersingsbenaderingen zoals cognitieve gedragstherapie (CGT), die is ontworpen om patiënten pijnbeheersingsvaardigheden te leren om hun pijn coping-strategieën te verbeteren en stress te verminderen die kan leiden tot meer pijn.
Klinische studies hebben aangetoond dat gedragsinterventies “pijn en invaliditeit kunnen verminderen voor patiënten met kanker,” zei Dr. Somers. “Maar CGT voor pijnbeheersing kan mensen ook vaardigheden aanreiken om met pijn om te gaan, zodat ze, zelfs als hun pijn op een bepaald niveau aanhoudt, kunnen blijven doen wat ze moeten doen, of willen doen, van dag tot dag.
“We weten dat deze copingvaardigheden mensen helpen hun pijn te beheersen,” vervolgde Dr. Somers. Maar gedragsmatige pijnbestrijding vereist meestal persoonlijke therapiesessies in een medisch centrum en een aanzienlijke tijdsbesteding, en “op veel plaatsen is er niet eens een therapeut beschikbaar die is opgeleid om deze interventies te doen,” zei ze.
Om deze uitdagingen aan te pakken, bestudeert Dr. Somers of een kortere of lagere “dosis” van een gedragsmatige pijninterventie nog steeds voordelen kan bieden. In een lopende, door het NCI gesponsorde klinische studie, onderzoekt zij de respons van borstkankerpatiënten met matige of ernstige pijn op verschillende doses van training in het omgaan met pijn. Het doel is om uit te vinden “wie welke dosis van een gedragsmatige kankerpijninterventie nodig heeft om er baat bij te hebben, met als einddoel deze aanpak toegankelijker te maken voor patiënten”, aldus Dr. Somers.
Dr. Somers kijkt ook naar alternatieven voor persoonlijke therapie voor mensen met chronische kankerpijn, waaronder mobiele gezondheidsinterventies. Dergelijke interventies kunnen videoconferenties en elektronische tabletkiosken in medische centra in de gemeenschap omvatten voor patiënten die thuis geen toegang hebben tot technologie, zoals medisch onderbedeelde bevolkingsgroepen in landelijke gebieden.
Een uitdaging bij het gebruik van gedragsinterventies om kankerpijn te beheersen, zei Dr. O’Mara, “is dat het, in tegenstelling tot het nemen van een pil, een inzet van tijd en inspanning van de patiënt vereist.” Een van de vragen is dan ook: “hoe kunnen we patiënten in staat stellen zich in te zetten voor deze benaderingen,” die de pijn misschien niet wegnemen, maar hen wel helpen ermee te leven, zei ze.
Andere uitdagingen bij het bestuderen en beheersen van pijn
Wanneer het op pijnbestrijding aankomt, verdient het de voorkeur vroeg in het ziekteverloop met de behandeling te beginnen – en idealiter voordat de pijn zich überhaupt ontwikkelt, zei Dr. Mantyh. Maar dat kan een uitdaging zijn, zei hij, omdat oncologen meer gericht zijn op “de behandeling van de tumor … en het kan moeilijk zijn om van hen de buy-in te krijgen om vroeg in de ziekte pijnbestrijding te geven.”
Eén zorg onder oncologen, zei Dr. Dougherty, is dat medicijnen om pijn te voorkomen kunnen interageren en interfereren met antikanker behandelingen. “Je wilt in de eerste plaats dat patiënten de therapie overleven, en een middel dat zou kunnen interageren met een kankertherapie zou een duidelijk nadeel hebben,” zei hij.
Hoe dan ook, voegde hij eraan toe, is het belangrijk om zenuwgerelateerde pijn zoals CIPN zo snel mogelijk aan te pakken, want als pijn eenmaal chronisch wordt, “begint het zenuwstelsel van een patiënt te veranderen en te proberen zich aan te passen aan die toestand … nu heb je een nieuw probleem om te proberen het zenuwstelsel terug te brengen naar waar het was.”
Een andere complicerende factor is dat mannen en vrouwen verschillende biologische reacties op pijn kunnen hebben, zei Dr. Dougherty. Zijn laboratorium vergelijkt menselijke sensorische neuronen van pijnlijke en niet-pijnlijke gebieden bij patiënten met CIPN om de biologische basis te onderzoeken. Nog niet gepubliceerde bevindingen geven aan dat, “zoals is gesuggereerd in dierstudies, er verschillen zijn tussen mannen en vrouwen” in de manier waarop neuronen reageren op door chemotherapie veroorzaakte stress, wat suggereert dat therapieën voor CIPN specifiek moeten worden afgestemd op basis van het geslacht van de patiënt, zei hij.
Eén ding is duidelijk, wetenschappers die op dit gebied werken zijn het erover eens: Het verbeteren van het begrip van pijn en het gebruik van die kennis om de ontdekking en ontwikkeling van nieuwe behandelingen te sturen, is van cruciaal belang voor het fysieke en mentale welzijn van patiënten.
“De meeste mensen zullen het ermee eens zijn dat als je de pijn kunt beheersen, dat waarschijnlijk een verschil zal maken in het verlengen van de levensduur van een patiënt, alleen al omdat ze in staat zijn om te sporten, een sociaal leven te onderhouden en proberen een gezonde levensstijl te behouden,” zei Dr. Mantyh. “Als je de functionele status van een kankerpatiënt kunt behouden, verbeter je hun levenskwaliteit enorm. En dat, samen met het in staat zijn om hun kankertherapieën te blijven volgen… is waar het allemaal om draait.”