導電性
イオン性化合物のもう一つの特徴的な性質は、その導電性です。
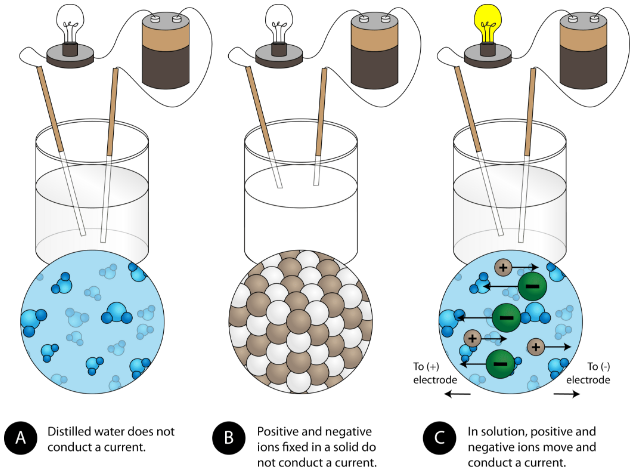
1つ目のビーカーでは、水は分子化合物なので蒸留水は電気を通しません。 2つ目のビーカーには、固体の塩化ナトリウムが入っていますが、これも電流は流れません。 イオン性の荷電粒子であるにもかかわらず、固体の結晶格子のためにイオンが電極間を移動できないのです。 回路が完成して電球が点灯するには、移動可能な荷電粒子が必要です。 3つ目のビーカーでは、NaClを蒸留水に溶かしました。 これで、結晶格子が分解され、個々の正イオンと負イオンが移動できるようになりました。 カチオンは一方の電極に、アニオンはもう一方の電極に移動し、電気が流れます(下図参照)。 また、イオン性化合物を溶かすと、イオンが解放されて電流が流れます。 イオン性化合物は、水に溶かしたり、溶かしたりすると電流が流れる。 イオン性化合物の水への溶解については、9.3.項で説明します
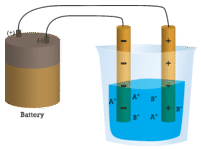
Example ˶(˶ˆ꒳ˆ˵ )
固体のNaClの水中での解離式を書いてください。
解答
NaCl(s) → Na+(aq) + Cl-(aq)
Exercise ˶(˶´⚰︎`˵)
固体のNH4NO3の水中での解離方程式を書きなさい。
Answer
NH4NO3(s) → NH4+(aq) + NO3-(aq)
Exercise!